Cancer gastrique : comprendre ses causes et explorer les options de traitement
Le cancer de l’estomac , également connu sous le nom de cancer gastrique, est un type de cancer qui prend naissance dans la muqueuse de l’estomac. C’est un problème de santé important dans le monde, avec environ 1 million de nouveaux cas et 783 000 décès chaque année. Le cancer de l’estomac se développe souvent lentement sur de nombreuses années et peut passer inaperçu à ses débuts, ce qui rend difficile son traitement efficace.
Il existe plusieurs facteurs de risque associés au cancer de l’estomac, notamment des antécédents familiaux de la maladie, une alimentation riche en aliments salés, fumés ou marinés et certaines conditions médicales telles que l’infection à Helicobacter pylori et la gastrite chronique. D’autres facteurs qui peuvent augmenter le risque de développer un cancer de l’estomac comprennent le tabagisme, la consommation d’alcool et l’obésité.
Les symptômes du cancer de l’estomac peuvent être non spécifiques et peuvent inclure des nausées, une perte d’appétit, des douleurs abdominales et une perte de poids involontaire. À mesure que le cancer progresse, des symptômes plus graves tels que du sang dans les selles, des vomissements et des difficultés à avaler peuvent survenir.
La détection précoce est cruciale pour le succès du traitement du cancer de l’estomac. Les options de traitement peuvent inclure la chirurgie, la chimiothérapie et la radiothérapie. De plus, des changements de mode de vie tels que l’adoption d’un régime alimentaire sain et l’arrêt du tabac peuvent aider à réduire le risque de développer un cancer de l’estomac.
Dans cet article, nous explorerons les causes, les facteurs de risque, les symptômes et les options de traitement du cancer de l’estomac, ainsi que les moyens de réduire votre risque de développer cette maladie.
Sommaire [ masquer ]
Introduction
A. Définition du cancer gastrique :
Le cancer gastrique, également connu sous le nom de cancer de l’estomac, est une tumeur maligne qui provient des cellules qui tapissent l’estomac. Ce type de cancer peut survenir dans n’importe quelle partie de l’estomac et peut se propager aux organes voisins ou se métastaser dans des parties éloignées du corps par la circulation sanguine ou le système lymphatique. Le cancer gastrique peut être classé en différents types histologiques, le plus courant étant l’adénocarcinome, qui représente environ 90 % de tous les cas. D’autres types comprennent le lymphome, les tumeurs stromales gastro-intestinales (GIST) et les tumeurs neuroendocrines.
B. Épidémiologie et prévalence mondiale :
Le cancer gastrique est le cinquième cancer le plus répandu dans le monde et la troisième cause de décès liés au cancer. L’incidence du cancer gastrique varie considérablement d’une région à l’autre, les taux les plus élevés étant observés en Asie de l’Est, en particulier dans des pays comme le Japon, la Chine et la Corée du Sud. D’autres régions avec des taux d’incidence élevés comprennent l’Europe de l’Est, l’Amérique centrale et du Sud et certaines parties de l’Afrique. L’incidence du cancer gastrique a diminué au cours des dernières décennies, en partie grâce à l’amélioration des conditions de vie et à un meilleur accès aux soins de santé. Cependant, il représente toujours un fardeau important pour la santé, en particulier dans les pays en développement.
C. Importance du dépistage et du traitement précoces :
La détection précoce et le traitement rapide du cancer gastrique sont cruciaux pour améliorer les résultats pour les patients. Lorsqu’il est détecté à un stade précoce, le cancer gastrique a plus de chances d’être traité avec succès et le taux de survie global peut être considérablement amélioré. Malheureusement, le cancer gastrique est souvent asymptomatique ou présente des symptômes non spécifiques à ses débuts, ce qui le rend difficile à diagnostiquer. En conséquence, de nombreux patients sont diagnostiqués à des stades avancés lorsque le cancer s’est propagé, et les options de traitement deviennent limitées. Une sensibilisation accrue au cancer gastrique, à ses facteurs de risque et à ses symptômes peut aider à promouvoir une détection précoce et une intervention rapide, améliorant ainsi le pronostic des patients touchés par cette maladie.
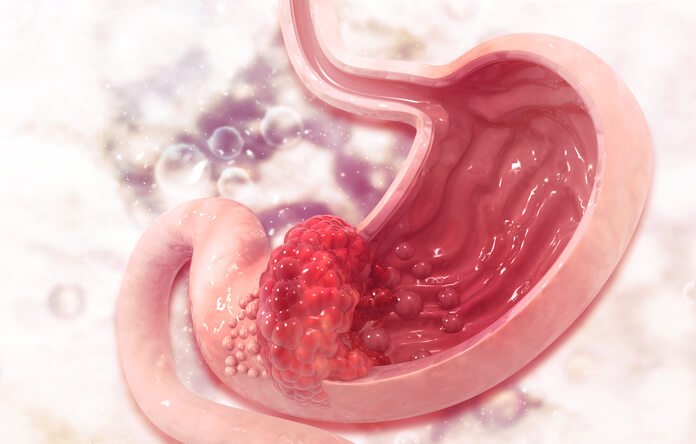
II. Causes et facteurs de risque
A. Facteurs génétiques :
Il existe des preuves que des facteurs génétiques jouent un rôle dans le développement du cancer gastrique. Alors que la plupart des cas de cancer gastrique sont sporadiques, environ 1 à 3 % des cas sont héréditaires et peuvent être attribués à des mutations génétiques spécifiques. Certains des syndromes héréditaires connus associés à un risque accru de cancer gastrique comprennent le cancer gastrique diffus héréditaire (HDGC), causé par des mutations du gène CDH1, et le syndrome de Lynch, également connu sous le nom de cancer colorectal héréditaire sans polypose (HNPCC). De plus, il existe des preuves que certaines variations génétiques courantes, connues sous le nom de polymorphismes mononucléotidiques (SNP), peuvent être associées à un risque plus élevé de cancer gastrique.
Infection à B. Helicobacter pylori :
L’infection à H. pylori est le facteur de risque le plus important du cancer gastrique. Cette bactérie colonise la muqueuse de l’estomac et peut provoquer une inflammation chronique, entraînant le développement d’une gastrite atrophique, d’une métaplasie intestinale et éventuellement d’un cancer gastrique. L’infection à H. pylori est responsable d’environ 75 % de tous les cas de cancer gastrique dans le monde. Cependant, tous les individus infectés par H. pylori ne développent pas un cancer gastrique, ce qui suggère que des facteurs supplémentaires, tels que la génétique de l’hôte et des facteurs environnementaux, peuvent influencer le développement de la maladie.
C. Facteurs liés à l’alimentation et au mode de vie :
Certains facteurs liés à l’alimentation et au mode de vie ont été associés à un risque accru de cancer gastrique. Ceux-ci incluent des régimes riches en sel, en viandes fumées ou transformées et pauvres en fruits et légumes. La consommation d’aliments contaminés par des nitrites et des nitrates, qui peuvent être convertis en nitrosamines cancérigènes dans l’estomac, peut également augmenter le risque. D’autres facteurs liés au mode de vie qui peuvent contribuer au cancer gastrique comprennent le tabagisme, la forte consommation d’alcool et l’obésité.
D. Facteurs environnementaux :
Des facteurs environnementaux, tels que l’exposition à certains produits chimiques ou substances, ont été impliqués dans le développement du cancer gastrique. Par exemple, l’exposition à l’amiante, aux rayonnements ionisants et à certains risques professionnels, comme le travail dans l’industrie du caoutchouc, a été associée à un risque accru de cancer gastrique. Cependant, ces facteurs contribuent à une faible proportion de cas de cancer gastrique par rapport à d’autres facteurs de risque, tels que l’infection à H. pylori et la prédisposition génétique.
E. Âge et sexe :
Le risque de développer un cancer gastrique augmente avec l’âge, la plupart des cas survenant chez les personnes de plus de 50 ans. Le cancer gastrique est également plus fréquent chez les hommes que chez les femmes, avec un ratio hommes-femmes d’environ 2:1.
F. Gastrite chronique et autres conditions médicales :
L’inflammation chronique de la muqueuse de l’estomac, connue sous le nom de gastrite, peut augmenter le risque de développer un cancer gastrique. En plus de l’infection à H. pylori, les autres causes de gastrite comprennent la gastrite auto-immune et l’utilisation à long terme d’anti-inflammatoires non stéroïdiens (AINS). Les patients atteints d’anémie pernicieuse , une affection qui entraîne une carence en vitamine B12 en raison de l’incapacité à absorber la vitamine, courent également un risque accru de cancer gastrique. D’autres conditions médicales qui ont été associées à un risque plus élevé de cancer gastrique comprennent les polypes gastriques et des antécédents de gastrectomie partielle.
III. Symptômes et diagnostic
A. Symptômes courants :
Aux premiers stades, le cancer gastrique ne provoque souvent aucun symptôme ou peut présenter des symptômes non spécifiques qui peuvent être confondus avec d’autres affections gastro-intestinales. Au fur et à mesure que le cancer progresse, les patients peuvent ressentir une gamme de symptômes, notamment :
1. Douleur ou gêne abdominale, généralement dans la partie supérieure de l’abdomen
2. Indigestion ou brûlures d’estomac
3. Perte d’appétit
4. Perte de poids involontaire
5. Nausées et vomissements, parfois accompagnés de sang
6. Difficulté à avaler ou sensation de coincement des aliments
7. Sentiment rassasié rapidement après avoir mangé, même de petites quantités de nourriture
8. Fatigue ou faiblesse
9. Anémie (faible nombre de globules rouges), souvent due à un saignement de la tumeur
10. Gonflement ou accumulation de liquide dans l’abdomen (ascite)
Il est essentiel de consulter un professionnel de la santé si l’un de ces symptômes persiste, car un diagnostic et un traitement précoces peuvent améliorer considérablement le pronostic du cancer gastrique.
B. Outils et techniques de diagnostic :
1. Endoscopie :
L’endoscopie est un outil diagnostique clé du cancer gastrique. Un tube flexible avec une lumière et une caméra à son extrémité, appelé endoscope, est inséré dans la bouche et dans l’œsophage pour examiner la muqueuse de l’estomac. La procédure permet au médecin de visualiser toute anomalie et d’obtenir des échantillons de tissus pour une analyse plus approfondie.
2. Biopsie :
Une biopsie consiste à prélever un petit échantillon de tissu de la zone suspecte de l’estomac pour l’examiner au microscope. Cela se fait généralement pendant la procédure d’endoscopie. Un pathologiste analyse l’échantillon de tissu pour déterminer si des cellules cancéreuses sont présentes et, le cas échéant, le type de cancer et son grade.
3. Techniques d’imagerie (tomodensitométrie, IRM, TEP) :
les techniques d’imagerie telles que la tomodensitométrie (TDM), l’imagerie par résonance magnétique (IRM) et la tomographie par émission de positrons (TEP) peuvent fournir des images détaillées de l’estomac et des structures environnantes. . Ces modalités d’imagerie aident à déterminer l’étendue du cancer, sa propagation aux organes voisins ou aux ganglions lymphatiques et la présence de métastases dans des parties éloignées du corps.
4. Tests sanguins :
Les tests sanguins peuvent fournir des informations sur l’état de santé général du patient et peuvent détecter la présence de certaines substances, appelées marqueurs tumoraux, qui peuvent être associées au cancer gastrique. Le marqueur tumoral le plus courant du cancer gastrique est l’antigène carcinoembryonnaire (CEA), bien qu’il ne soit pas spécifique au cancer gastrique et qu’il puisse également être élevé dans d’autres conditions.
C. Stadification du cancer gastrique :
Une fois le cancer gastrique diagnostiqué, il est essentiel de déterminer le stade de la maladie, qui indique à quel point le cancer est avancé et s’il s’est propagé à d’autres parties du corps. La stadification est basée sur la taille de la tumeur (T), l’implication des ganglions lymphatiques voisins (N) et la présence de métastases à distance (M). La stadification joue un rôle essentiel dans la détermination du plan de traitement le plus approprié et dans la prédiction du pronostic du patient. Le système de stadification couramment utilisé pour le cancer gastrique est le système TNM développé par l’American Joint Committee on Cancer (AJCC).
IV. Approches de traitement
Une opération:
La chirurgie est souvent le traitement principal du cancer gastrique, en particulier aux premiers stades de la maladie. Le type de chirurgie dépend de l’emplacement, de la taille et du stade de la tumeur.
1. Types de chirurgie :
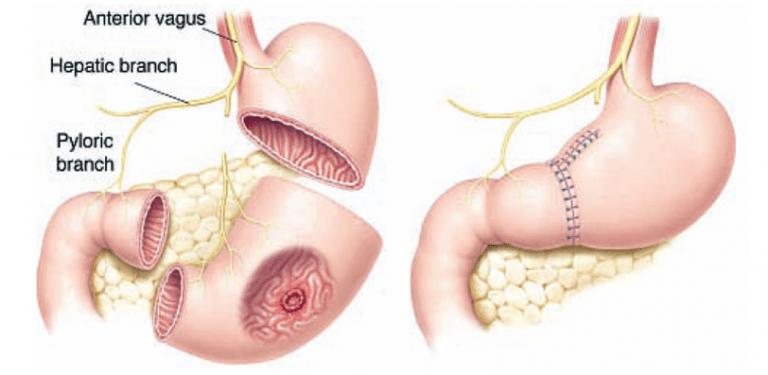
un. Gastrectomie subtotale : cette procédure consiste à retirer la partie de l’estomac affectée par la tumeur, ainsi que les ganglions lymphatiques voisins et parfois des parties d’autres organes si le cancer s’est propagé. La partie saine restante de l’estomac est ensuite reliée à l’intestin grêle.
b. Gastrectomie totale : Dans cette procédure, tout l’estomac est enlevé avec les ganglions lymphatiques voisins et parfois des parties d’autres organes si le cancer s’est propagé. L’œsophage est alors directement relié à l’intestin grêle.
c. Résection endoscopique : Cette procédure peu invasive convient aux cancers gastriques à un stade très précoce qui ne se sont pas propagés au-delà de la paroi interne de l’estomac. Le tissu cancéreux est retiré à l’aide d’un endoscope, sans qu’il soit nécessaire de recourir à une chirurgie ouverte.
2. Risques et avantages :
La chirurgie peut être curative si le cancer est détecté à un stade précoce et ne s’est pas propagé à d’autres organes ou tissus. Cependant, la chirurgie comporte des risques inhérents, tels que des saignements, des infections et des complications liées à l’anesthésie. De plus, les patients qui ont subi une gastrectomie peuvent ressentir des effets secondaires à long terme, tels que des difficultés à manger, une malabsorption des nutriments et une perte de poids.
B. Chimiothérapie :
La chimiothérapie utilise des médicaments pour tuer les cellules cancéreuses ou arrêter leur croissance. Il peut être utilisé avant la chirurgie (thérapie néoadjuvante) pour réduire la taille de la tumeur, ce qui facilite son retrait, ou après la chirurgie (thérapie adjuvante) pour éliminer les cellules cancéreuses restantes et réduire le risque de récidive.
1. Chimiothérapie néoadjuvante et adjuvante :
a. Une chimiothérapie néoadjuvante est administrée avant la chirurgie pour rétrécir la tumeur et augmenter la probabilité d’une ablation chirurgicale complète. Cette approche peut également rendre possible des techniques chirurgicales moins invasives.
b. Une chimiothérapie adjuvante est administrée après la chirurgie pour tuer toutes les cellules cancéreuses restantes, réduisant ainsi le risque de récidive du cancer. La décision d’utiliser une chimiothérapie adjuvante dépend du stade du cancer et du risque de récidive.
2. Effets secondaires et prise en charge :
La chimiothérapie peut provoquer divers effets secondaires, tels que nausées, vomissements, perte de cheveux, fatigue et risque accru d’infection. La plupart des effets secondaires sont temporaires et peuvent être gérés avec des médicaments et des soins de soutien. Les effets secondaires spécifiques ressentis dépendent du type et de la posologie des agents chimiothérapeutiques utilisés.
C. Radiothérapie :
La radiothérapie utilise des rayons ou des particules à haute énergie pour détruire les cellules cancéreuses. Il peut être utilisé avant la chirurgie pour rétrécir la tumeur ou après la chirurgie pour tuer les cellules cancéreuses restantes.
1. Radiothérapie externe :
Il s’agit du type de radiothérapie le plus courant pour le cancer gastrique. Une machine à l’extérieur du corps dirige des faisceaux de haute énergie sur le site de la tumeur. Le traitement est généralement administré en séances quotidiennes sur plusieurs semaines.
2. Curiethérapie :
En curiethérapie, des graines ou des pastilles radioactives sont placées directement dans ou à proximité de la tumeur. Cette approche permet d’administrer une dose de rayonnement plus élevée directement aux cellules cancéreuses, minimisant ainsi les dommages aux tissus sains environnants. La curiethérapie est moins couramment utilisée pour le cancer gastrique mais peut être envisagée dans des situations spécifiques.
3. Effets secondaires et prise en charge :
La radiothérapie peut provoquer des effets secondaires tels qu’une irritation de la peau, de la fatigue, des nausées, des vomissements et de la diarrhée. La plupart des effets secondaires sont temporaires et peuvent être gérés avec des médicaments et des soins de soutien. Les effets secondaires à long terme peuvent inclure des dommages aux organes et aux tissus voisins.
D. Thérapie ciblée et immunothérapie :
Ces nouvelles options de traitement visent à cibler des caractéristiques spécifiques des cellules cancéreuses ou à améliorer la réponse immunitaire de l’organisme contre les cellules cancéreuses.
1. Anticorps monoclonaux :
Les anticorps monoclonaux sont des protéines fabriquées en laboratoire qui peuvent cibler des protéines spécifiques sur les cellules cancéreuses ou dans l’environnement environnant, interférant avec la croissance et la survie des cellules cancéreuses. Le trastuzumab (Herceptin) est un anticorps monoclonal utilisé pour traiter le cancer gastrique HER2-positif, un sous-type de la maladie avec une surexpression de la protéine HER2.
2. Inhibiteurs de points de contrôle immunitaires :
Les inhibiteurs de points de contrôle immunitaires sont un type d’immunothérapie qui aide le système immunitaire à reconnaître et à attaquer les cellules cancéreuses. Ces médicaments bloquent les protéines qui agissent comme des « freins » sur les cellules immunitaires, permettant au système immunitaire de cibler et de détruire plus efficacement les cellules cancéreuses. Des exemples d’inhibiteurs de points de contrôle immunitaires utilisés dans le traitement du cancer gastrique comprennent le pembrolizumab (Keytruda) et le nivolumab (Opdivo), qui ciblent la protéine PD-1.
3. Thérapies émergentes et essais cliniques :
De nouvelles thérapies ciblées et immunothérapies sont continuellement développées et testées dans des essais cliniques. Ces essais visent à identifier des options de traitement plus efficaces et moins toxiques pour le cancer gastrique. Les patients atteints d’un cancer gastrique avancé ou récurrent qui ont épuisé les options de traitement standard peuvent envisager de s’inscrire à un essai clinique.
E. Soins palliatifs et gestion des symptômes :
Les soins palliatifs sont un aspect essentiel du traitement du cancer gastrique, en particulier pour les patients atteints d’une maladie avancée ou métastatique. L’objectif des soins palliatifs est d’améliorer la qualité de vie du patient en gérant les symptômes, tels que la douleur, la nausée et la difficulté à manger, et en répondant aux préoccupations émotionnelles, spirituelles et pratiques. Les soins palliatifs peuvent être fournis parallèlement à d’autres traitements contre le cancer et doivent être adaptés aux besoins et aux préférences de chaque patient.
V. Prévention et détection précoce
A. Stratégies de prévention primaire :
La prévention primaire vise à réduire le risque de développer un cancer gastrique en s’attaquant aux facteurs de risque modifiables et en favorisant un mode de vie sain.
1. Éradication de H. pylori :
Le dépistage et le traitement de l’infection à H. pylori peuvent aider à prévenir le cancer gastrique, car la bactérie est responsable de la majorité des cas. Les antibiotiques peuvent éradiquer efficacement l’infection à H. pylori et réduire le risque de développer un cancer gastrique, surtout s’ils sont traités à un stade précoce de l’infection.
2. Modifications alimentaires :
Adopter une alimentation saine peut réduire le risque de cancer gastrique. Cela comprend une alimentation riche en fruits et légumes, en grains entiers et en protéines maigres tout en limitant la consommation de sel, de viandes transformées et d’aliments fumés ou marinés. Consommer des aliments riches en antioxydants et autres nutriments anticancéreux peut également aider à protéger contre le cancer gastrique.
3. Contrôle du tabac et de l’alcool :
L’arrêt du tabac et la limitation de la consommation d’alcool peuvent réduire le risque de développer un cancer gastrique. Les politiques de santé publique et les interventions visant à réduire la consommation de tabac et d’alcool peuvent jouer un rôle crucial dans la prévention du cancer gastrique au niveau de la population.
4. Maintenir un poids santé :
L’obésité est un facteur de risque de cancer gastrique, et le maintien d’un poids santé grâce à une alimentation équilibrée et à une activité physique régulière peut aider à réduire ce risque.
B. Détection et dépistage précoces :
La détection précoce du cancer gastrique peut améliorer considérablement les chances de succès du traitement et de survie à long terme. Cependant, le dépistage systématique du cancer gastrique n’est actuellement pas recommandé pour la population générale dans la plupart des pays, car les avantages ne l’emportent pas sur les risques et les coûts pour les personnes à risque moyen.
1. Populations à haut risque :
Le dépistage peut être envisagé pour les personnes à haut risque de cancer gastrique, telles que celles qui ont de forts antécédents familiaux de la maladie, des syndromes de cancer gastrique héréditaire ou une infection connue à H. pylori. Dans certains pays à forte incidence de cancer gastrique, comme le Japon et la Corée du Sud, des programmes de dépistage de masse ont été mis en place à l’aide d’endoscopie gastro-intestinale haute et/ou de tests de déglutition barytés.
2. Sensibilisation et éducation :
Accroître la sensibilisation du public au cancer gastrique, à ses facteurs de risque et à ses symptômes peut aider à promouvoir une détection précoce et une intervention rapide. Les prestataires de soins de santé doivent éduquer leurs patients sur les signes avant-coureurs du cancer gastrique et les encourager à consulter un médecin s’ils présentent des symptômes persistants ou préoccupants.
3. Avancées dans les techniques de diagnostic :
Les techniques de diagnostic émergentes, telles que les méthodes endoscopiques peu invasives, les tests sanguins pour les marqueurs tumoraux et les biomarqueurs moléculaires, pourraient améliorer la détection précoce du cancer gastrique à l’avenir. La recherche et le développement en cours dans ce domaine pourraient aider à identifier des outils de diagnostic plus sensibles et spécifiques pouvant être utilisés pour le dépistage et la détection précoce dans les populations à haut risque.